APOIE mensalmente e tenha acesso imediato à versão digital, sempre!
ou
ASSINE e receba a revista impressa na sua casa
Notícias Recentes
VER MAIS NOTÍCIASArtigos
Veja mais Artigos
Eu Digo X: Cuidando de quem cuida
Pixbay / Creative Commons

Eu Digo X: Desenvolvimento motor na aprendizagem é tema de simpósio
Reprodução / Divulgação

‘E todos lavam as mãos’
Depositphotos
Revista Autismo é qualidade de informação, é isenção, é pioneirismo no mundo!
Primeiro periódico, em língua portuguesa, especializado em transtorno do espectro do autismo (TEA), a missão da Revista Autismo é disseminar o conhecimento que transforma e faz tanta diferença no dia a dia dos autistas, seus familiares e profissionais.

Mais Notícias
VER MAIS NOTÍCIAS
Acesse os conteúdos exclusivos da Revista Autismo digital
O autismo não é simples! Seus desafios e características revelam-se de diferentes formas ao longo da vida, porque cada ser humano é único.
O tema é importante, é urgente! Acompanhe nossas edições trimestrais e aprofunde-se sobre esse complexo universo.
Mais Lidas

Messi não é autista
Fake news foi criada no Brasil em 2013 e circula até hoje n...
 Revista Autismo / Canal Autismo
Revista Autismo / Canal Autismo
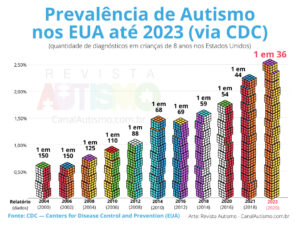
Prevalência de autismo: 1 em 36 é o novo número do CDC nos EUA
Atualizada a cada 2 anos nos Estados Unidos, pesquisa considera...
 Reprodução / Folha de S.Paulo
Reprodução / Folha de S.Paulo
Maior nota em matemática do Enem 2023 é de estudante autista
O estudante Alexandre Andrade de Almeida, de 16 anos, alcançou a nota máxima na prova de Matemáti...
por Canal Autismo

Entrevista com Mauricio de Sousa: 20 anos do André
Em entrevista exclusiva, o pai da Turma da Mônica fala de inclu...
 Depositphotos
Depositphotos
Por que o Brasil pode ter 6 milhões de autistas?
Para ser exato, podemos ter hoje pelo menos 5.997.222 pessoas au...
 Depositphotos
Depositphotos
Psiquiatra fala de suicídio e autismo em vídeo da Tismoo.me
Você sabia que o índice de suicídio entre pessoas autistas cerca de 8 vezes maior em comparação...



 por Sabrina Muggiati
por Sabrina Muggiati por Paula Ayub
por Paula Ayub
 por Sophia Mendonça
por Sophia Mendonça

 por Haydée Jacques Freire
por Haydée Jacques Freire











